
Генная терапия: как лечат генетические заболевания
---
Одни из самых страшных заболеваний, которыми «одаривает» человека природа, – это заболевания генетические. Можно успешно бороться с возбудителями недугов – бактериями и вирусами, но, если проблема находится в геноме человека от рождения, помочь пациенту крайне тяжело. Современная наука упорно ищет возможность «отремонтировать» мутировавшие гены.

Миодистрофия Дюшенна — одно из нечасто встречающихся, но все же относительно распространенных генетических заболеваний. Болезнь диагностируется в трех-пятилетнем возрасте, обычно у мальчиков, проявляясь поначалу лишь в затрудненных движениях, к десяти годам страдающий такой миодистрофией уже не может ходить, к 20−22 годам его жизнь заканчивается. Она вызвана мутацией гена дистрофина, который находится в Х-хромосоме. Он кодирует белок, соединяющий мембрану мышечной клетки с сократительными волокнами. Функционально это своеобразная пружина, обеспечивающая плавное сокращение и целостность клеточной мембраны. Мутации в гене приводят к дистрофии скелетных мышечных тканей, диафрагмы и сердца. Лечение заболевания носит паллиативный характер и позволяет лишь немного облегчить страдания. Однако с развитием генной инженерии появился свет в конце тоннеля.
О войне и мире
Генная терапия — это доставка внутрь клетки конструкций на основе нуклеиновых кислот для лечения генетических заболеваний. С помощью такой терапии можно исправить генетическую проблему на уровне ДНК и РНК, меняя процесс экспрессии нужного белка. Например, в клетку можно доставить ДНК с исправленной последовательностью, с которой синтезируется функциональный белок. Или, напротив, возможны удаления определенных генетических последовательностей, что также поможет уменьшить вредные последствия мутации. В теории это просто, однако на практике генная терапия базируется на сложнейших технологиях работы с объектами микромира и представляет собой совокупность передовых ноу-хау в области молекулярной биологии.

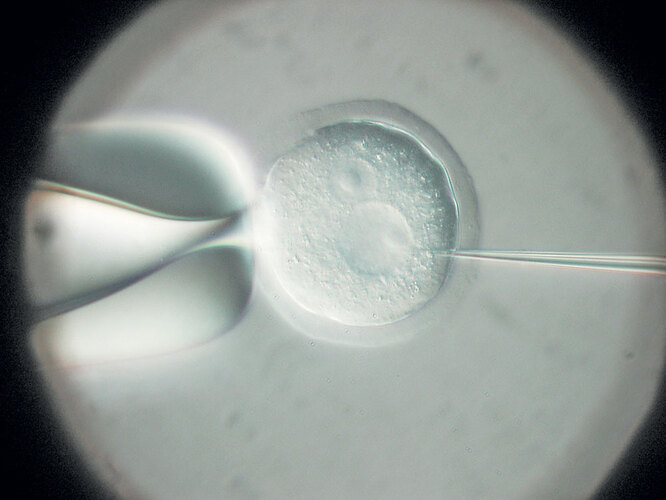
Инъекция ДНК в пронуклеус зиготы — одна из самых ранних и наиболее традиционных технологий создания трансгенов. Инъекция производится вручную с помощью сверхтонких игл под микроскопом с 400-кратным увеличением.
«Ген дистрофина, мутации которого порождают миодистрофию Дюшенна, огромный, — рассказывает директор по развитию биотехнологической компании "Марлин Биотех", кандидат биологических наук Вадим Жерновков. — Он включает в себя 2,5 млн пар нуклеотидов, что можно было бы сравнить с количеством букв в романе "Война и мир". И вот представим себе, что мы вырвали из эпопеи несколько каких-то важных страниц. Если на этих страницах описываются существенные события, то понимание книги было бы уже затруднено. Но с геном все сложнее. Найти другую копию "Войны и мира" несложно, и тогда недостающие страницы можно было бы прочитать. Но ген дистрофина находится в X-хромосоме, а у мужчин она одна. Таким образом, в половых хромосомах у мальчиков при рождении хранится лишь одна копия гена. Другую взять негде.

Наконец, при синтезе белка из РНК важно сохранение рамки считывания. Рамка считывания определяет, какая группа из трех нуклеотидов считывается как кодон, что соответствует одной аминокислоте в белке. Если произошло удаление в гене фрагмента ДНК, не кратное трем нуклеотидам, происходит сдвиг рамки считывания — кодировка изменяется. Это можно было бы сравнить с ситуацией, когда после вырванных страниц во всей оставшейся книге все буквы заменятся на следующие по алфавиту. Получится абракадабра. Вот то же самое происходит с неправильно синтезируемым белком».
Биомолекулярный пластырь
Один из эффективных методов генной терапии для восстановления нормального синтеза белка — пропуск экзонов с помощью коротких нуклеотидных последовательностей. В «Марлин Биотех» уже отработана технология работы с геном дистрофина с помощью такого метода. Как известно, в процессе транскрипции (синтеза РНК) сначала формируется так называемая прематричная РНК, заключающая в себе как кодирующие белок участки (экзоны), так и некодирующие (интроны). Далее начинается процесс сплайсинга, в ходе которого интроны и экзоны разъединяются и формируется «зрелая» РНК, состоящая только из экзонов. В этот момент некоторые экзоны можно заблокировать, «залепить» с помощью особых молекул. В итоге в зрелой РНК не окажется тех кодирующих участков, от которых мы предпочли бы избавиться, и таким образом восстановится рамка считывания, белок будет синтезироваться.

«Эту технологию мы отладили in vitro, — рассказывает Вадим Жерновков, то есть на клеточных культурах, выращенных из клеток пациентов с миодистрофией Дюшенна. Но отдельные клетки — это не организм. Вторгаясь в процессы клетки, мы должны наблюдать последствия вживую, однако привлечь к испытаниям людей не представляется возможным по разным причинам — от этических до организационных. Поэтому возникла необходимость получения модели миодистрофии Дюшенна с определенными мутациями на основе лабораторного животного».
Как уколоть микромир
Трансгенные животные — это полученные в лаборатории животные, в геном которых целенаправленно, осознанно внесены изменения. Еще в 70-е годы прошлого века стало понятно, что создание трансгенов — это важнейший метод исследования функций генов и белков. Одним из самых ранних методов получения полностью генно-модифицированного организма стала инъекция ДНК в пронуклеус («предшественник ядра») зигот оплодотворенных яйцеклеток. Это логично, так как модифицировать геном животного проще всего в самом начале его развития.
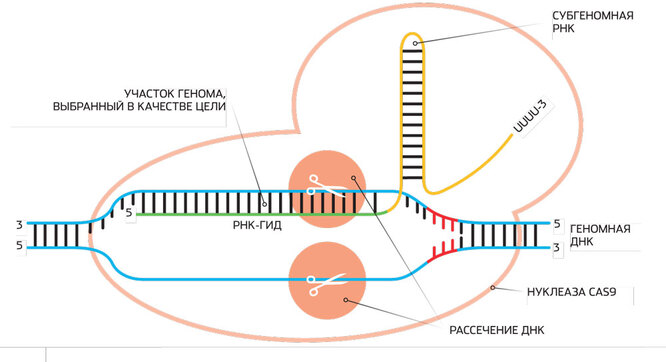
На схеме продемонстрирован процесс CRISPR/Cas9, в котором участвуют субгеномная РНК (sgRNA), ее участок, работающий как РНК-гид, а также белок-нуклеаза Cas9, который рассекает обе нити геномной ДНК в указанном РНК-гидом месте.
Инъекция в ядро зиготы — весьма нетривиальная процедура, ведь речь идет о микромасштабах. Яйцеклетка мыши имеет диаметр 100 мкм, а пронуклеус — 20 мкм. Операция происходит под микроскопом с 400-кратным увеличением, однако инъекция — это самая что ни на есть ручная работа. Разумеется, для «укола» применяется не традиционный шприц, а специальная стеклянная игла с полым каналом внутри, куда набирается генный материал. Один ее конец можно держать в руке, а другой — сверхтонкий и острый — практически не виден невооруженным глазом. Конечно, такая хрупкая конструкция из боросиликатного стекла не может храниться долго, поэтому в распоряжении лаборатории есть набор заготовок, которые непосредственно перед работой вытягиваются на специальном станке. Используется особая система контрастной визуализации клетки без окрашивания — вмешательство в пронуклеус само по себе травматично и является фактором риска для выживания клетки. Краска стала бы еще одним таким фактором. К счастью, яйцеклетки достаточно живучи, однако количество зигот, которые дают начало трансгенным животным, составляют лишь несколько процентов от общего числа яйцеклеток, в которые была сделана инъекция ДНК.
Следующий этап — хирургический. Проводится операция по трансплантации микроинъецированных зигот в воронку яйцевода мыши-реципиента, которая станет суррогатной матерью будущим трансгенам. Далее лабораторное животное естественным путем проходит цикл беременности, и на свет появляется потомство. Обычно в помете находится около 20% трансгенных мышат, что также говорит о несовершенстве метода, ибо в нем присутствует большой элемент случайности. При инъекции исследователь не может контролировать, как именно внедренные фрагменты ДНК встроятся в геном будущего организма. Высока вероятность таких комбинаций, которые приведут к гибели животного еще на эмбриональной стадии. Тем не менее метод работает и вполне годен для ряда научных целей.

Развитие трансгенных технологий позволяет производить животные белки, востребованные фармацевтической промышленностью. Эти белки экстрагируются из молока трансгенных коз и коров. Также есть технологии получения специфических белков из куриного яйца.
Ножницы для ДНК
Но есть более эффективный способ на основе целевого редактирования генома по технологии CRISPR/Cas9. «Сегодня молекулярная биология в чем-то подобна эпохе дальних морских экспедиций под парусами, — говорит Вадим Жерновков. — Практически каждый год в этой науке происходят значительные открытия, которые могут изменить нашу жизнь. Например, несколько лет назад микробиологи обнаружили у давно, казалось бы, изученного вида бактерий иммунитет к вирусным инфекциям. В результате дальнейших исследований выяснилось, что ДНК бактерий содержат в себе особые локусы (CRISPR), с которых синтезируются фрагменты РНК, умеющие комплементарно связываться с нуклеиновыми кислотами чужеродных элементов, например с ДНК или РНК вирусов. С такой РНК связывается белок Cas9, представляющий собой фермент-нуклеазу. РНК служит для Cas9 гидом, помечающим определенный участок ДНК, в котором нуклеаза совершает разрез. Примерно три-пять лет назад появились первые научные труды, в которых разрабатывалась технология CRISPR/Cas9 для редактирования генома».

Трансгенные мыши позволяют создавать живые модели тяжелых генетических заболеваний человека. Люди должны быть благодарны этим крохотным существам.
По сравнению со способом введения конструкции для случайного встраивания, новый метод позволяет подобрать элементы системы CRISPR/Cas9 таким образом, чтобы точно нацелить РНК-гиды на нужные участки генома и добиться целенаправленной делеции или вставки нужной последовательности ДНК. В этом методе тоже возможны ошибки (РНК-гид иногда соединяется не с тем участком, на который его нацеливают), однако при использовании CRISPR/Cas9 эффективность создания трансгенов составляет уже около 80%. «Этот метод имеет широкие перспективы, и не только для создания трансгенов, но и в других областях, в частности в генной терапии, — говорит Вадим Жерновков. — Однако технология находится только в начале пути, и представить себе, что в ближайшее время исправлять генный код людей будут с помощью CRISPR/Cas9, довольно сложно. Пока есть вероятность ошибки, есть и опасность, что человек лишится какой-то важной кодирующей части генома».

Молоко-лекарство
Российской компании «Марлин Биотех» удалось создать трансгенную мышь, в которой полностью воспроизведена мутация, приводящая к миодистрофии Дюшенна, и следующим этапом станут испытания технологий генной терапии. Вместе с тем создание моделей генетических заболеваний человека на основе лабораторных животных — не единственное возможное применение трансгенов. Так, в России и западных лабораториях ведутся работы в области биотехнологий, позволяющие получать важные для фарминдустрии лекарственные белки животного происхождения. В качестве продуцентов могут выступать коровы или козы, у которых можно изменять клеточный аппарат производства содержащихся в молоке белков. Из молока можно экстрагировать лекарственный белок, который получен не химическим способом, а с помощью природного механизма, что повысит эффективность лекарства. В настоящее время разработаны технологии получения таких лекарственных белков, как лактоферрин человека, проурокиназа, лизоцим, атрин, антитромбин и другие.

Миодистрофия Дюшенна — одно из нечасто встречающихся, но все же относительно распространенных генетических заболеваний. Болезнь диагностируется в трех-пятилетнем возрасте, обычно у мальчиков, проявляясь поначалу лишь в затрудненных движениях, к десяти годам страдающий такой миодистрофией уже не может ходить, к 20−22 годам его жизнь заканчивается. Она вызвана мутацией гена дистрофина, который находится в Х-хромосоме. Он кодирует белок, соединяющий мембрану мышечной клетки с сократительными волокнами. Функционально это своеобразная пружина, обеспечивающая плавное сокращение и целостность клеточной мембраны. Мутации в гене приводят к дистрофии скелетных мышечных тканей, диафрагмы и сердца. Лечение заболевания носит паллиативный характер и позволяет лишь немного облегчить страдания. Однако с развитием генной инженерии появился свет в конце тоннеля.

О войне и мире
Генная терапия — это доставка внутрь клетки конструкций на основе нуклеиновых кислот для лечения генетических заболеваний. С помощью такой терапии можно исправить генетическую проблему на уровне ДНК и РНК, меняя процесс экспрессии нужного белка. Например, в клетку можно доставить ДНК с исправленной последовательностью, с которой синтезируется функциональный белок. Или, напротив, возможны удаления определенных генетических последовательностей, что также поможет уменьшить вредные последствия мутации. В теории это просто, однако на практике генная терапия базируется на сложнейших технологиях работы с объектами микромира и представляет собой совокупность передовых ноу-хау в области молекулярной биологии.

Инъекция ДНК в пронуклеус зиготы — одна из самых ранних и наиболее традиционных технологий создания трансгенов. Инъекция производится вручную с помощью сверхтонких игл под микроскопом с 400-кратным увеличением.
«Ген дистрофина, мутации которого порождают миодистрофию Дюшенна, огромный, — рассказывает директор по развитию биотехнологической компании "Марлин Биотех", кандидат биологических наук Вадим Жерновков. — Он включает в себя 2,5 млн пар нуклеотидов, что можно было бы сравнить с количеством букв в романе "Война и мир". И вот представим себе, что мы вырвали из эпопеи несколько каких-то важных страниц. Если на этих страницах описываются существенные события, то понимание книги было бы уже затруднено. Но с геном все сложнее. Найти другую копию "Войны и мира" несложно, и тогда недостающие страницы можно было бы прочитать. Но ген дистрофина находится в X-хромосоме, а у мужчин она одна. Таким образом, в половых хромосомах у мальчиков при рождении хранится лишь одна копия гена. Другую взять негде.

Наконец, при синтезе белка из РНК важно сохранение рамки считывания. Рамка считывания определяет, какая группа из трех нуклеотидов считывается как кодон, что соответствует одной аминокислоте в белке. Если произошло удаление в гене фрагмента ДНК, не кратное трем нуклеотидам, происходит сдвиг рамки считывания — кодировка изменяется. Это можно было бы сравнить с ситуацией, когда после вырванных страниц во всей оставшейся книге все буквы заменятся на следующие по алфавиту. Получится абракадабра. Вот то же самое происходит с неправильно синтезируемым белком».
Биомолекулярный пластырь
Один из эффективных методов генной терапии для восстановления нормального синтеза белка — пропуск экзонов с помощью коротких нуклеотидных последовательностей. В «Марлин Биотех» уже отработана технология работы с геном дистрофина с помощью такого метода. Как известно, в процессе транскрипции (синтеза РНК) сначала формируется так называемая прематричная РНК, заключающая в себе как кодирующие белок участки (экзоны), так и некодирующие (интроны). Далее начинается процесс сплайсинга, в ходе которого интроны и экзоны разъединяются и формируется «зрелая» РНК, состоящая только из экзонов. В этот момент некоторые экзоны можно заблокировать, «залепить» с помощью особых молекул. В итоге в зрелой РНК не окажется тех кодирующих участков, от которых мы предпочли бы избавиться, и таким образом восстановится рамка считывания, белок будет синтезироваться.

«Эту технологию мы отладили in vitro, — рассказывает Вадим Жерновков, то есть на клеточных культурах, выращенных из клеток пациентов с миодистрофией Дюшенна. Но отдельные клетки — это не организм. Вторгаясь в процессы клетки, мы должны наблюдать последствия вживую, однако привлечь к испытаниям людей не представляется возможным по разным причинам — от этических до организационных. Поэтому возникла необходимость получения модели миодистрофии Дюшенна с определенными мутациями на основе лабораторного животного».
Как уколоть микромир
Трансгенные животные — это полученные в лаборатории животные, в геном которых целенаправленно, осознанно внесены изменения. Еще в 70-е годы прошлого века стало понятно, что создание трансгенов — это важнейший метод исследования функций генов и белков. Одним из самых ранних методов получения полностью генно-модифицированного организма стала инъекция ДНК в пронуклеус («предшественник ядра») зигот оплодотворенных яйцеклеток. Это логично, так как модифицировать геном животного проще всего в самом начале его развития.

На схеме продемонстрирован процесс CRISPR/Cas9, в котором участвуют субгеномная РНК (sgRNA), ее участок, работающий как РНК-гид, а также белок-нуклеаза Cas9, который рассекает обе нити геномной ДНК в указанном РНК-гидом месте.
Инъекция в ядро зиготы — весьма нетривиальная процедура, ведь речь идет о микромасштабах. Яйцеклетка мыши имеет диаметр 100 мкм, а пронуклеус — 20 мкм. Операция происходит под микроскопом с 400-кратным увеличением, однако инъекция — это самая что ни на есть ручная работа. Разумеется, для «укола» применяется не традиционный шприц, а специальная стеклянная игла с полым каналом внутри, куда набирается генный материал. Один ее конец можно держать в руке, а другой — сверхтонкий и острый — практически не виден невооруженным глазом. Конечно, такая хрупкая конструкция из боросиликатного стекла не может храниться долго, поэтому в распоряжении лаборатории есть набор заготовок, которые непосредственно перед работой вытягиваются на специальном станке. Используется особая система контрастной визуализации клетки без окрашивания — вмешательство в пронуклеус само по себе травматично и является фактором риска для выживания клетки. Краска стала бы еще одним таким фактором. К счастью, яйцеклетки достаточно живучи, однако количество зигот, которые дают начало трансгенным животным, составляют лишь несколько процентов от общего числа яйцеклеток, в которые была сделана инъекция ДНК.
Следующий этап — хирургический. Проводится операция по трансплантации микроинъецированных зигот в воронку яйцевода мыши-реципиента, которая станет суррогатной матерью будущим трансгенам. Далее лабораторное животное естественным путем проходит цикл беременности, и на свет появляется потомство. Обычно в помете находится около 20% трансгенных мышат, что также говорит о несовершенстве метода, ибо в нем присутствует большой элемент случайности. При инъекции исследователь не может контролировать, как именно внедренные фрагменты ДНК встроятся в геном будущего организма. Высока вероятность таких комбинаций, которые приведут к гибели животного еще на эмбриональной стадии. Тем не менее метод работает и вполне годен для ряда научных целей.

Развитие трансгенных технологий позволяет производить животные белки, востребованные фармацевтической промышленностью. Эти белки экстрагируются из молока трансгенных коз и коров. Также есть технологии получения специфических белков из куриного яйца.
Ножницы для ДНК
Но есть более эффективный способ на основе целевого редактирования генома по технологии CRISPR/Cas9. «Сегодня молекулярная биология в чем-то подобна эпохе дальних морских экспедиций под парусами, — говорит Вадим Жерновков. — Практически каждый год в этой науке происходят значительные открытия, которые могут изменить нашу жизнь. Например, несколько лет назад микробиологи обнаружили у давно, казалось бы, изученного вида бактерий иммунитет к вирусным инфекциям. В результате дальнейших исследований выяснилось, что ДНК бактерий содержат в себе особые локусы (CRISPR), с которых синтезируются фрагменты РНК, умеющие комплементарно связываться с нуклеиновыми кислотами чужеродных элементов, например с ДНК или РНК вирусов. С такой РНК связывается белок Cas9, представляющий собой фермент-нуклеазу. РНК служит для Cas9 гидом, помечающим определенный участок ДНК, в котором нуклеаза совершает разрез. Примерно три-пять лет назад появились первые научные труды, в которых разрабатывалась технология CRISPR/Cas9 для редактирования генома».

Трансгенные мыши позволяют создавать живые модели тяжелых генетических заболеваний человека. Люди должны быть благодарны этим крохотным существам.
По сравнению со способом введения конструкции для случайного встраивания, новый метод позволяет подобрать элементы системы CRISPR/Cas9 таким образом, чтобы точно нацелить РНК-гиды на нужные участки генома и добиться целенаправленной делеции или вставки нужной последовательности ДНК. В этом методе тоже возможны ошибки (РНК-гид иногда соединяется не с тем участком, на который его нацеливают), однако при использовании CRISPR/Cas9 эффективность создания трансгенов составляет уже около 80%. «Этот метод имеет широкие перспективы, и не только для создания трансгенов, но и в других областях, в частности в генной терапии, — говорит Вадим Жерновков. — Однако технология находится только в начале пути, и представить себе, что в ближайшее время исправлять генный код людей будут с помощью CRISPR/Cas9, довольно сложно. Пока есть вероятность ошибки, есть и опасность, что человек лишится какой-то важной кодирующей части генома».

Молоко-лекарство
Российской компании «Марлин Биотех» удалось создать трансгенную мышь, в которой полностью воспроизведена мутация, приводящая к миодистрофии Дюшенна, и следующим этапом станут испытания технологий генной терапии. Вместе с тем создание моделей генетических заболеваний человека на основе лабораторных животных — не единственное возможное применение трансгенов. Так, в России и западных лабораториях ведутся работы в области биотехнологий, позволяющие получать важные для фарминдустрии лекарственные белки животного происхождения. В качестве продуцентов могут выступать коровы или козы, у которых можно изменять клеточный аппарат производства содержащихся в молоке белков. Из молока можно экстрагировать лекарственный белок, который получен не химическим способом, а с помощью природного механизма, что повысит эффективность лекарства. В настоящее время разработаны технологии получения таких лекарственных белков, как лактоферрин человека, проурокиназа, лизоцим, атрин, антитромбин и другие.
Источник: polonsil.ru
Комментарии (0)
{related-news}
[/related-news]